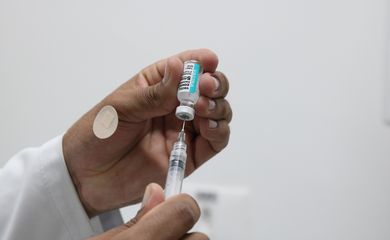
Anvisa analisa uso emergencial de nova vacina contra covid-19

Um pedido de Autorização de Uso Emergencial para a versão da vacina bivalente contra a covid-19, desenvolvida pelo laboratório farmacêutico Moderna e comercializada pela Adium, foi apresentado à Agência Nacional de Vigilância Sanitária (Anvisa), nesta sexta-feira (17).

As vacinas bivalentes são desenvolvidas com tecnologia mRNA, utilizando a sequência do vírus e não através da inserção de uma versão enfraquecida ou inativada do vírus em si. "A vacina cria a capacidade para que o corpo crie uma proteína que imita uma parte do novo vírus. Neste processo, as células do corpo constroem proteínas que são acrescentadas ao sistema imunológico. As células imunológicas notam que estas são proteínas estranhas e reagem gerando uma resposta para proteger contra o vírus", segundo a fabricante.
Segundo a Anvisa, esse tipo de vacina promete conferir maior proteção à variante Ômicron, quando comparada com vacinas monovalentes. Por sua transmissibilidade, observa a agência, a variante Ômicron causa preocupação às autoridades sanitárias do país.
A Adium havia apresentado o pedido de registro da vacina, em janeiro. "Este pedido se encontra em análise pela equipe técnica da Anvisa. Porém, a empresa decidiu protocolar a Autorização de Uso Emergencial, paralelamente ao pedido do registro, de acordo com a manifestação favorável do Ministério da Saúde, conforme previsto no parágrafo único do Art. 1º da Resolução (RDC) 688, de 13 de maio de 2022", explicou a agência, em nota.
Uso Emergencial
Uma vez recebido o pedido de Autorização de Uso Emergencial, a Anvisa tem 30 dias para concluir sua avaliação. Esse prazo é interrompido sempre que for necessário solicitar à empresa a complementação de informações ou esclarecimentos sobre os dados de qualidade, de eficácia e de segurança apresentados.
*Matéria foi alterada às 15h15 do dia 8 de março para correção da composição da vacina bivalente. Diferentemente do publicado, a vacina bivalente não contém uma mistura de cepas do vírus SARS-Cov-2.